4.3. Технология ионного обмена
В технологии водоподготовки применяются два основных процесса для удаления из воды ионизированных примесей: катионирование и анионирование. В зависимости от обменного иона процессы и аппараты называют: натрий-катионирование, натрий-катионитный фильтр; H (водород)-катионирование, H-катионитный фильтр; OH-анионирование, OH-анионитный фильтр. Соответственно называется фильтрат, полученный в этих процессах: Na-катионированная вода, H-катионированная вода, OH-анированная вода и т.п. Процессы Na-катионирование имеет самостоятельное значение и используется для умягчения воды, в то время как процессы H- и OH-ионирование реализуются совместно в схемах обессоливания воды.
Н-катионирование может осуществляться в схемах H-Na-катионирования воды. Процессы ионирования воды на водоподготовительных установках реализуются в насыпных ионитных фильтрах раздельного и смешанного действия.
Na-катионирование. Этот процесс применяют для умягчения воды путем фильтрования ее через слой катионита в натриевой форме. При этом ионы Ca2+ и Mg2+, обуславливающие жесткость исходной воды, задерживаются катионитом в обмен на эквивалентное количество ионов Na2+:
| 2RNa + Ca2+ « R2Ca + 2Na+, |
(4.6) |
| 2RNa + Mg2+ « R2Mg + 2Na+, |
(4.7) |
где R - матрица с фиксированными зарядами без обменного иона, считающаяся одновалентной.
Остаточная жесткость фильтра при Na-катионировании может быть получена при надлежащих условиях регенерации фильтра на уровне 5 - 10 мкг-экв/дм3, что является определяющим при реализации этого процесса.
Анионный состав Na-катионированной воды остается неизменным, поэтому карбонатная жесткость исходной воды переходит в гидрокарбонат натрия, что можно пояснить реакцией:
| Ca(HCO3)2 + 2NaR ® R2Ca + 2NaHCO3. |
(4.8) |
Это соединение, попадая с подпиточной водой в котел, превращается в конечном итоге в гидроксид натрия по реакциям:
| 2NaHCO3 + H2O ® Na2CO3 + CO2 + H2O, |
(4.9) |
| Na2CO3 + H2O ® 2NaOH + CO2, |
(4.10) |
который может инициировать щелочную коррозию.
Неизменность величины щелочности при Na-катионировании является основным недостатком этого процесса, поэтому он может иметь самостоятельное значение только при подготовке воды для подпитки теплосети и добавочной воды для котлов низкого и среднего давлений при сравнительно низкой щелочности исходной воды. Второй недостаток рассматриваемой технологии определяется увеличением солесодержания фильтрата при выражении его в массовых единицах, что связано с эквивалентными массами ионов Na+ (23 единицы), Ca2+ (20 единиц) и Mg2+ (12 единиц). Напомним, что ионный обмен характеризуется эквивалентностью, поэтому из воды удаляются ионы с меньшей эквивалентной массой (Ca2+, Mg2+), а их место занимает ион натрия с большей эквивалентной массой.
Процесс умягчения при Na-катионировании заканчивается при наступлении проскока жесткости (рис. 4.10), после чего истощенный катионит в фильтре надо регенерировать, т.е. восстанавливать его способность к обмену ионами. Регенерацию истощенного катионита проводят пропуском через него 6 - 10% раствора NaCl. Вследствие относительно большой концентрации ионов Na+ в регенерационном растворе происходит замена ими поглощенных ранее катионов Ca2+ и Mg2+ по реакциям:
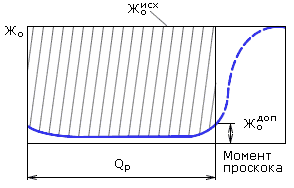
Рис. 4.10. Выходная кривая Na-катионитного фильтра
| R2Ca + nNa+ « 2RNa + Ca2+ + (n - 2)Na+, |
(4.11) |
| R2Mg + nNa+ « 2RNa + Mg + (n - 2)Na+, |
(4.12) |
где n - избыток NaCl против его стехиометрического расхода.
Несмотря на то, что процесс обмена ионов, в том числе и при регенерации ионита, характеризуется эквивалентностью, для качественной регенерации ионитов расход реагента выбирается с определенным избытком (n). При подаче раствора соли в фильтр лучше будет отрегенерирован лобовой катионита, контактирующий со свежим раствором. По мере прохождения раствора в глубинные части катионита условия регенерации будут ухудшаться вследствие повышения концентрации в регенерационном растворе ионов Ca2+ и Mg2+, вытесненных из верхних слоев катионита при обеднении регенеранта ионами Na+. Аналогичное действие проявляется за счет загрязнения раствора технической NaCl ионами Ca2+ и Mg2+.
Эффект прироста обменной емкости с увеличением расхода соли при регенерации показан на рис. 4.11, из которого следует, что эффект прироста обменной емкости с увеличением удельного расхода более 300 г/г-экв заметно снижается. Поясним, что 300 г NaCl на 1 г-экв вытесняемых ионов жесткости при эквивалентной массе NaCl равной 58.5 г соответствует 300/58.5 = 5.13 г-экв избытка соли, т.е. n = 5.13 г-экв/г-экв. На практике расход соли на регенерацию принимают в пределах 120 - 140 г/г-экв по экономическим и экологическим соображениям, поэтому рабочая обменная емкость (Eр) не достигает значения полной. Ограничение расхода соли позволяет уменьшить ее количество в сточных регенерационных водах, так как непосредственно на вытеснение из катионита 1 г-экв поглощенных ионов расходуется 1 г-экв ионов натрия. Таким образом, в сточных водах будет содержаться для рассматриваемых условий (n = 2.4 г-экв/г-экв = 140 г/г-экв) на каждый вытесненный 1 г-экв ионов Ca2+ и Mg2+ - 1.4 г-экв ионов Na+ и 2.4 г-экв ионов Cl-.
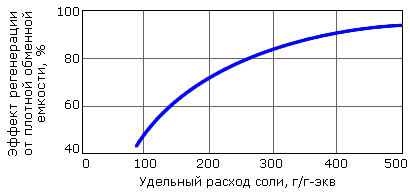
Рис. 4.11. Влияние расхода соли на эффект регенерации катионита
Эффект регенерации катионита при выбранном расходе реагента повышается с увеличением продолжительности контакта раствора соли с катионитом, поэтому скорость пропуска регенерационного раствора ограничивают пределами 4 - 6 м/ч при высоте слоя катионита 1.5 - 2.0 м. Скорость ниже 4.0 м/ч не используется по гидродинамическим условиям работы фильтра.
Регенерацию ионита в фильтрах можно проводить несколькими способами, которые отличаются друг от друга направлениями потоков обрабатываемой воды и регенерационного раствора. При совпадении направлений потока воды и регенерационного раствора, подаваемых обычно сверху - вниз, регенерацию называют параллельно-точной, такая регенерация создает невыгодные условия для процесса умягчения из-за распределения ионов Na+ и ионов жесткости в слое отрегенерированного материала (рис. 4.12, а). На выходе из слоя катионита умягчаемая вода, в которой резко снижена концентрация ионов жесткости, проходит через участки плохо отрегенерированного катионита и поэтому не может глубоко умягчаться. Кроме того, такое обстоятельство может привести к переходу некоторой части ионов жесткости из катионита в воду. При противоточной регенерации регенерационный раствор подается в направлении, противоположном подаче потока обрабатываемой воды, при этом наиболее полно регенерируются выходные (по воде) слои катионита (рис. 4.12, б). Это позволяет не только сохранить постоянное значение остаточной концентрации ионов в фильтрате, но и получить фильтрат более высокого качества при сниженных избытках реагента и, следовательно, меньших объемах сточных вод. Эффективная противоточная технология позволяет сократить количество ступеней очистки воды за счет повышения качества фильтрата. К недостатку противоточной регенерации относится усложнение конструкции фильтра, связанное с недопущением перемешивания слоев ионита при подаче раствора или воды в нижнюю часть фильтра.
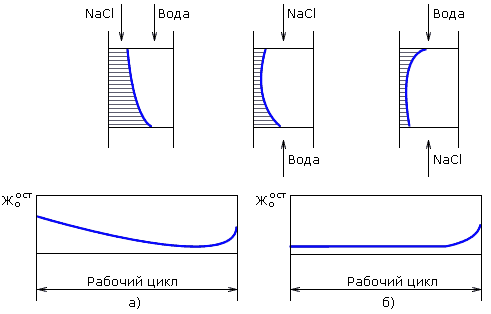
Рис. 4.12. Характер изменения остаточных концентраций ионов Ca2+ и Mg2+ в слое катионита и остаточная жесткость фильтрата при прямоточной (а) и противоточной (б) регенерациях
Для сокращения расхода реагентов с использованием параллельно-точной технологии регенерации применяют двухступенчатую схему Na-катионирования, т.е. последовательное включение двух фильтров. Фильтр 1 ст. регенерируется с относительно наибольшем избытком NaCl (n = 1.8 - 2.4), поэтому остаточная жесткость фильтрата получается высокой, на уровне 0.1 мг-экв/дм3. Фильтр 2 ст. регенерируется с 6.5 - 7.5-кратным избытком соли, поэтому остаточная жесткость воды снижается со 100 до 5 - 10 мкг-экв/дм3. Технико-экономические расчеты показали, что, несмотря на увеличение количества фильтров в двухступенчатой схеме, последняя имеет преимущества перед одноступенчатой схемой за счет снижения расхода NaCl при равноценном качестве умягченной воды.
H-катионирование. Обработка воды методом H-катионирования предназначается для удаления всех катионов из воды с заменой их на ионы водорода. Вода за H-катионитными фильтрами содержит избыток ионов водорода и вследствие этого имеет кислую реакцию, поэтому эта технология применяется совместно с другими процессами ионирования - Na-катионированием или анионированием. Обмен катионов при H-катионировании протекает согласно реакциям:
| 2RH + Ca2+ « R2Ca + 2H+, |
(4.13) |
| 2RH + Mg2+ « R2Mg + 2H+, |
(4.14) |
| RH + Na+ « RNa + H+. |
(4.15) |
Выделяющиеся ионы H+ реагируют в обрабатываемой воде с гидрокарбонатными ионами:
| H+ + HCO3 « CO2 + H2O. |
(4.16) |
Остаточная кислотность фильтрата после завершения реакции (4.16) с учетом равенства эквивалентных концентраций катионов и анионов будет равна:
| CH+ = (SАн - СHCO3-)исх = (СSO42- + CCl-)исх, |
(4.17) |
что позволяет контролировать полноту обмена ионов при H-катионировании по кислотности и по известным показателям качества поступающей на фильтр воды. При наличии в исходной воде ионов NO3 - и NO2 - они также должны быть учтены в расчетной оценке кислотности H-катионированной воды.
Сорбция катионов Ca2+, Mg2+ и Na+ ионитом осуществляется в соответствие с расположением этих ионов в ряду селективности (Ca2+ > Mg2+ > Na+), поэтому в слое H-катионита сверху располагается зона поглощения иона Ca2+, ниже - иона Mg2+ и далее - иона Na+. Эти три зоны по мере истощения H-катионита передвигаются одна за другой по направлению к нижней границе слоя ионита и первым обнаружится проскок иона Na+.
В работе H-катионитного фильтра можно выделить два основных периода (рис. 4.13):
- Полное поглощение всех катионов (абсцисса Oa). Фильтрат имеет кислотность, равную (СCl- + СSO42-)исх. В точке a наблюдается проскок иона Na+.
- Появление нарастающей концентрации иона Na+. В этот период концентрация иона Na+ постепенно возрастает, а кислотность начинает снижаться за счет уменьшения количества вытесняемых ионов H+. К моменту достижения начального содержания иона Na+ в исходной воде его поглощение прекращается, но происходит обмен в катионите ионов Ca2+ и Mg2+ исходной воды на сорбированный катионитом ион Na+ до его полного вытеснения. В этот момент (точка E) появляется проскок жесткости.
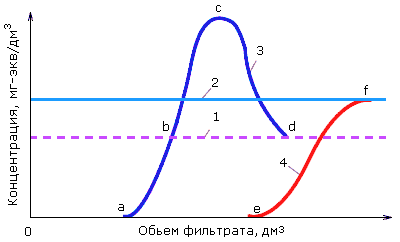
Рис. 4.13. Изменение качества H-катионированной воды:
1 – концентрация Na+ в исходном растворе; 2 – жесткость исходного раствора; 3 – концентрация Na+ в фильтрате; 4 – жесткость фильтрата; точки: a – проскок Na+, b – отсутствие поглощения Na+, c – максимум вытеснения Na+ из катионита, d – окончание вытеснения Na+, e – начало проскока жесткости, f – выравнивание жесткости в фильтрате и в исходном растворе
Параллельно с указанными выше изменениями концентрации катионов кислотность фильтрата после проскока ионов Na сначала уменьшается и достигает нуля, затем появляется возрастающая щелочность, достигающая исходных значений при обмене ионов Ca2+ и Mg2+ на Na+. Эффект умягчения воды при H-катионировании обычно столь же полный, как и при Na-катионировании.
Работа фильтра до проскока ионов Na+ или ионов жесткости зависит от технологической схемы его использования, соответственно изменяется его рабочая обменная емкость при работе до проскока ионов Na+ или жесткости.
Для регенерации истощения H-катионита по технико-экономическим соображениям в условиях России используется обычно H2SO4 концентрацией 1.0 - 1.5% (на некоторых установках применяются HCl и HNO3). Процесс регенерации характеризуется следующими реакциями:
| R2Ca + nH+ « 2RH + Ca2+ + (n - 2)H+. |
(4.18) |
| R2Mg + nH+ « 2RH + Mg2+ + (n - 2)H+, |
(4.19) |
| RNa + nH+ « RH + Na+ + (n - 1)H+. |
(4.20) |
Ограничение концентрации раствора H2SO4 связано с возможностью выделения на зернах регенерируемого катионита трудно растворимого CaSO4, т.е. его загипсовывания. Следующим мероприятием для борьбы с загипсовыванием катионита является ограничение времени контакта регенерационного раствора с катионитом, что реализуется на практике увеличением скорости пропуска 1.5%-ного раствора H2SO4 до не менее 10 м/ч.
Расход реагента существенно снижается, а качество фильтрата повышается при применении противоточной регенерации ионитного фильтра, схема которого приведена на рис. 4.14.
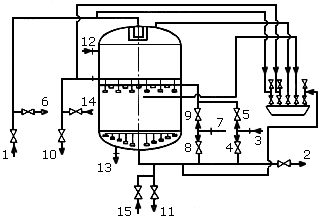
Рис. 4.14. Схема противоточного ионитного фильтра ФИПр:
1 – подвод исходной воды; 2 – отвод обработанной воды; 3 – подвод промывочной воды общий; 4 – подвод промывочной воды в нижнее распределительное устройство (РУ); 5 – подвод промывочной воды в блокирующее РУ; 6 – отвод промывочной воды; 7 – подвод регенерационного раствора в нижнее РУ; 9 – подвод регенерационного раствора в блокирующее РУ; 10, 11 – дренаж; 12 – гидрозагрузка; 13 – гидровыгрузка; 14 – подвод воды для взрыхления в среднее РУ; 15 – подвод воды для взрыхления в нижнее РУ
3D модель
Конструкция фильтра, изготавливаемого на ТКЗ предусматривает кроме верхнего и нижнего распределительных устройств (РУ), также среднее и блокирующее РУ, расположенные соответственно на глубине 0.3 м и у входной поверхности слоя ионита. Среднее распределительное устройство предназначено для равномерного сбора отработанного регенерационного раствора и отмывочной воды, подаваемых через нижнее (80%) и блокирующее РУ (20%). Блокирующее РУ служит для подвода раствора реагента или отмывочной воды, используемых одновременно для регенерации и зажатия блокирующего слоя ионита. Взрыхлению подвергается только блокирующий слой ионита, а через 10 - 20 фильтроциклов взрыхляется весь слой.
Промежуточным вариантом между противоточной и прямоточной регенерацией является двухпоточно-противоточная регенерация, осуществляемая в фильтре по схеме, приведенной на рис. 4.15. Среднее РУ заглублено в ФИПр-2П на 0.6 и 1.0 м соответственно для фильтров, загруженных анионитом или катионитом. Конструкция двухпоточно-противоточного фильтра позволяет использовать его как в режиме однопоточного фильтрования и двухпоточной регенерации, так и в режиме двухпоточного фильтрования и однопоточной регенерации. При любом режиме работы в выходном слое ионита осуществляется принцип противоточного ионирования, при котором обрабатываемая вода перед выходом из фильтра соприкасается с хорошо отрегенерированными слоями ионита, благодаря чему обеспечивается высокое качество фильтрата при сокращенных расходах реагентов на регенерацию ионита. При работе фильтра в режиме двухпоточного фильтрования взрыхлению подвергается весь слой ионита, при однопоточном фильтровании - только верхний слой, а взрыхление всего слоя производится через 10 - 20 фильтроциклов. При работе фильтра в режиме однопоточного фильтрования и двухпоточной регенерации 40% раствора реагента пропускается через верхний слой ионита, 60% - через нижний. При режиме двухпоточного фильтрования и однопоточной регенерации весь регенерационный раствор проходит через оба слоя ионита сверху - вниз.
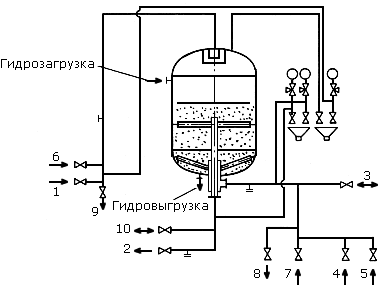
Рис. 4.15. Схема двухпоточно-противоточного ионитного фильтра ФИПр-2П:
1 – подвод исходной воды; 2 – отвод обработанной воды или отработанного регенерационного раствора и отмывочной воды; 3 – подвод исходной воды или отвод отработанной воды; 4 – подвод регенерационного раствора; 5 – подвод воды для взрыхления; 6 – подвод регенерационного раствора и отмывочной воды; 7 – подвод отмывочной воды; 8 – отвод отработанного регенерационного раствора и отмывочной воды; 9 – дренаж; 10 – подвод взрыхляющей воды, дренаж
Значения оптимального удельного расхода серной кислоты в зависимости от содержания в исходной воде Cl- и SO42- ионов, определяющих величину противоионного эффекта, показаны на рис. 4.16 применительно к H-катионитным фильтрам 1 ст. при параллельном токе и противотоке. Помимо экономии серной кислоты, при противотоке снижается содержание ее в сбросных регенерационных водах, что облегчает нейтрализацию сбросов.
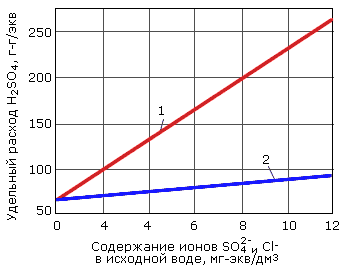
Рис. 4.16. Удельный расход серной кислоты на регенерацию H-фильтров 1 ступени:
1 – параллельный ток; 2 – противоток
Теоретические представления о динамике ионного обмена в совокупности с обработкой экспериментальных данных позволили обобщить влияние различных факторов на время наступления проскока заданных концентраций примесей в ионитных фильтрах. Расчетное уравнение для выходной кривой ионирования на катионите КУ-2-8 имеет вид:
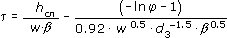 , , |
(4.21) |
где t - время фильтрования до заданной величины проскока, ч; w - скорость фильтрования, м/ч; d - диаметр зерна катионита, мм; hсл - высота слоя катионита, м; j = Cф/C0; b = C0/q0; C0 и Cф - концентрации иона соответственно исходная и в фильтрате; q0 - концентрация иона, сорбированного единицей объема катионита.
Уравнение (4.21) получено на кафедре ТВТ МЭИ (ТУ) А.А. Громогласовым.
Анионирование воды ведется с целью замены удаляемых анионов на ион гидроксила. При сочетании ОН-анионирования с Н-катионированием происходит удаление из воды как анионов, так и катионов в обмен на ионы ОН- и Н+, т.е. осуществляется химическое (ионитное) обессоливание воды. При фильтровании через слой анионита осуществляется сорбция анионов согласно реакциям:
| ROH + Cl- « RCl + OH-, |
(4.22) |
| 2ROH + SO42- « R2SO4 + 2OH-. |
(4.23) |
Высокое значение pH в зоне обмена на анионите способствует диссоциации слабых кислот H2CO3 и H2SiO3 и переводу их в ионизированное состояние, поэтому они также могут участвовать в реакциях анионного обмена, но лишь при использовании сильноосновных анионитов:
| ROH + H+ + HCO3- « RHCO3 + H2O, |
(4.24) |
| ROH + H+ + HSiO3 « RHSiO3 + H2O. |
(4.25) |
С учетом значений обменных емкостей слабоосновных и сильноосновных анионитов (EАН ³ EАВ), а также способности только последних сорбировать анионы слабых кислот, схемы химического обессоливания обычно включают две ступени анионирования: на первой в фильтры загружается слабоосновный анионит, удаляющие ионы SO42- и Cl-; на второй ступени в фильтры загружается сильноосновный анионит, предназначенный главным образом для обескремнивания воды.
Согласно ряду селективности в анионитном фильтре 1 ст. первыми проскакивают в фильтрат ионы Cl-, поэтому время выхода на регенерацию этого фильтра сопоставляют с концентрацией хлоридов; отключение анионитных фильтров 2 ст. на регенерацию проводят на основании контроля фильтрата по кремнекислоте.
Регенерация анионитных фильтров производится 4%-ным раствором NaOH, при этом происходят следующие реакции:
| RCl + nOH- « ROH + Cl - + (n - 1)OH-, |
(4.26) |
| R2SO4 + nOH- « 2ROH + SO42- + (n - 2)OH-, |
(4.27) |
| RHCO3 + nOH- « ROH + HCO3- + (n - 1)OH-, |
(4.28) |
| RHSiO3 + nOH- « ROH + HSiO3- + (n - 1)OH-. |
(4.29) |
Избыток щелочи (n) при регенерации слабоосновных анионитов при поглощении ими анионов сильных кислот достаточен в двукратном размере против стехиометрического количества, т.е. 80 г/г-экв. Для регенерации анионита, насыщенного анионами кремниевой кислоты, требуется повышенный избыток NaOH (n = 10 - 20), обеспечивающий последующее кремнесодержание фильтрата на уровне 0.1 мг/дм3 (рис. 4.17). Для снижения удельного расхода щелочи регенерацию параллельно-точных анионитных фильтров 2 и 1 ступеней проводят последовательно, либо используют противоточную или ступенчатопротивоточную технологию.
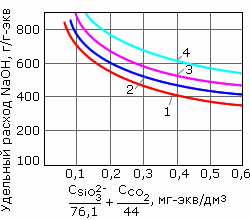
Рис. 4.17. Удельный расход NaOH на регенерацию анионита АВ-17 при обескремнивании воды:
1, 2 3, 4 – остаточное кремнесодержание фильтрата, соответственно 0.16; 0.12; 0.10; 0.08 мг/дм3 при расходе NaOH 100, 120, 150, 200 кг/м3
При проектировании технологии химического обессоливания учитывают, что наличие в H-катионированной воде свободной углекислоты, более сильной, чем кремниевая, уменьшает кремнеемкость анионита и вызывает более ранний проскок ионов HSiO3 - в фильтрат. Поэтому перед поступлением H-катионированной воды на слой сильноосновного анионита из нее необходимо возможно более полно удалить CO2, для чего в схему включается декарбонизатор. Еще сильнее снижает кремнеемкость анионита наличие в H-катионированной воде ионов Na+, так как помимо истощения анионита анионами, уравновешивающими эти катионы, увеличивается концентрация в фильтрате противоионов (OH-), что резко ухудшает глубину обескремнивания воды. С учетом приведенных фактов схемы обессоливания создаются, как правило, в виде двухступенчатых, содержащих основное оборудование, приведенное на рис. 4.18.
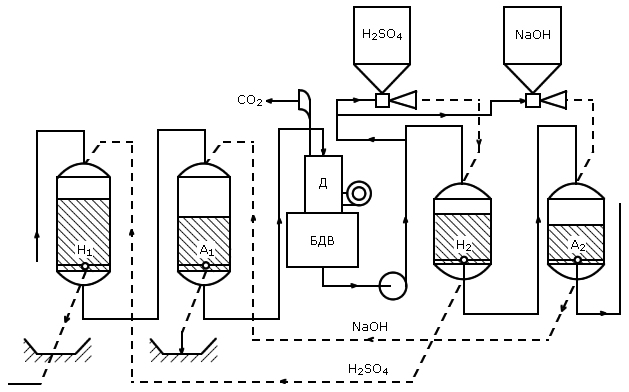
Рис. 4.18. Принципиальная схема двухступенчатого химического обессоливания:
H1 и H2 – катионитные фильтры 1-ой и 2-ой ступеней; A1 и A2 – анионитные фильтры 1-ой и 2-ой ступеней с загрузкой соответственно низкоосновными и высокоосновными анионитами, Д – декарбонизатор, БДВ – бак декарбонизованной (частично обессоленной) воды; H2SO4 – кислота для регенерации H-катионитных фильтров; NaOH – едконатриевая щелочь для регенерации OH-анионитных фильтров
Установки двухступенчатого химического обессоливания надежны в работе. Они обеспечивают высокое качество обработанной воды, отвечающее эксплуатационным нормам питательной воды барабанных котлов сверхвысокого давления.
Для очистки добавочной воды для прямоточных котлов и ядерных реакторов применяются трехступенчатые схемы химического обессоливания, в которых в качестве третьей ступени используются фильтры смешанного действия (ФСД). Загрузка ФСД состоит из смеси (от 2 ¸ 1 до 1 ¸ 2) сильнокислотного катионита а Н-форме и сильноосновного анионита в OH-форме. Переходящие в раствор в процессах ионного обмена на чередующихся зернах катионита и анионита ионы H+ и OH- образуют воду, выводя из зоны ионного обмена противоионы, способствуя этим углублению степени обессоливания воды до остаточной удельной электропроводимости менее 0.2 мкСм/см. Недостаток этой технологии заключается в необходимости тщательно перемешивать и разделять (при регенерации) составные части смешанной загрузки.








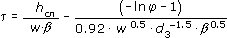 ,
,
