Уважаемый Валерий Федорович!
С Вашей статьей «Проблема единиц концентрации и ее решение в среде Mathcad» я знаком уже давно. Полностью разделяю Вашу точку зрения о том, что безусловное выполнение требований системы СИ может нанести (и уже наносит) определенный вред. Это относится, в том числе и к изгнанию из химических расчетов ставших «незаконными» единиц измерения, в частности, связанных с понятием «эквивалент». Проблема жесткости воды, описанная Вами в статье, не является единичной. Могу привести и другие примеры из собственной практики.
Предлагаю студентам на практикуме простую задачу: ведут электролиз раствора FeSO4. Вычислить массу железа, выделившегося на катоде, если через цепь пропущено количество электричества, равное 100 Кл? Большинство студентов специальности «Химия и основы информатики», которым на первой паре я прочитал, скажем, законы электролиза, а на второй – работу с размерностями в среде Mathcad, составят приблизительно такой документ:
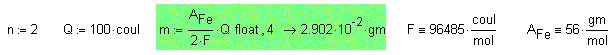
И за такой документ, содержащий
абсолютно верный окончательный результат, это самое большинство будет нещадно
мною преследоваться. Многие будут возражать, мол, здесь все верно. И дело даже
не в том, что атомная масса железа выражена в г/моль, а не
в требуемых СИ кг/(103моль). Это мелочь, на которую
химики по сей день не обращают (слава богу!) никакого внимания. Гораздо важнее,
в каких единицах представлена постоянная Фарадея F. “Это кулоны на моль!” – вопиет аудитория и демонстрирует
таблицу «Некоторые фундаментальные физико-химические постоянные» из «Химической
энциклопедии», где черным по белому (или, как поговаривают на военной кафедре,
«черным по русскому») действительно написано, что константа Фарадея выражается
в Кл/моль. Аргумент
«неэнциклопедистов»: число
электронов n – величина
безразмерная, делением размерной величины AFe на безразмерную получаем величину той же
размерности. Следовательно, с учетом размерности Q выходит, что [F]= Кл/моль… Приходится снова обращаться к
закону Фарадея и снова выяснять, что в самой формулировке этого закона заложены
эквиваленты. Число электронов – это то самое число структурных единиц, сидящих
в понятии «моль». Вот это и есть те самые «штуки», делением на которые обычная
молярная масса моль/л
превращается в молярную массу эквивалента. Против такой редакции документа я уже претензий иметь не буду:

Предложенный Вами прием использования механизма изменения стиля переменной Mathcad с целью получения результата, не противоречащего физическому смыслу и одновременно удовлетворяющему требованиям СИ, весьма удачен и достоин дальнейшего применения (рис. 3 Вашей статьи). Однако позволю предположить, что проблема этим не исчерпывается. Рис. 3 в значительной степени маскирует ее (примерно так, как иногда в среде Mathcad мы маскируем численные вычисления под символьную математику). А как быть пользователю в том случае, когда ион трех-, четырех-, пяти- и.т. д. многозарядный? Иметь на каждый случай одноименную переменную разного стиля? Вряд ли это рационально. Все равно это не освобождает пользователя от необходимости иметь представление о том, что такое эквивалент и что такое эквивалентная (нормальная) концентрация. Проблема (скорее, беда) в другом и кроется она не в том, что в СИ нет места другим концентрациям, кроме молярной (а между прочим, молярная концентрация моль/л тоже незаконна, должно быть моль/м3), а в том, что мы всегда очень законопослушны и любое нововведение воспринимаем через призму всевозможных запретов. Наверное, это генетическое. Да, в молях. Но разве кто-нибудь запрещал конкретизировать при этом «моль чего?», т. е. о каких структурных единицах идет речь. А ведь структурная единица – понятие вполне законное в СИ.
Так что Ваш коллега, очень похожий на чеховского персонажа, зря хватается за сердце и грозится уйти на пенсию (уверен, что не уйдет, это я вам как заведующий кафедрой заявляю). У меня на кафедре многие по нескольку раз на дню туда собираются, но так никто и не ушел.
Беда в том, что запреты вольно или невольно возводятся в абсолют. Примеры? Пожалуйста, постоянная Фарадея потеряла эквиваленты. Более грустный пример – это когда эквиваленты исключаются из вузовской программы. Долгое время основным учебником по общей химии для нехимических специальностей был знаменитый учебник Глинки. Недавно я узнал, что в России вышел новый учебник, в котором уже нет места эквивалентам. Ату его, эквивалент! Наверное, потому, что кто-то запреты СИ воспринял буквально. Вот и будем вскоре иметь и замерзшие водоемы, и еще чего похлеще.
Что касается терминологии статьи, я бы убрал из нее ссылки на «грамм-молекулу» и «грамм-эквивалент». Эти термины сейчас практически не используются (даже преподавателями с очень большим стажем) и заменены соответственно на «молярную массу» и молярную массу эквивалента». Кстати, хотел посмотреть определение термина «моль» в «Химической энциклопедии» (М.: изд-во «Большая российская энциклопедия», 1992,. Т. 3, С. 130-131) и обнаружил, что за статьей «Молочная кислота» сразу следует «моляльность, см. Концентрация». О моле забыли…
Насколько я понял, материал статьи выложен только на сайте. В каком издании Вы планируете ее опубликовать? По моему мнению, статья неплохо бы смотрелась в «Химии и жизни». Не знаю только, как тамошняя редакция относится к математическим пакетам и к Mathcad в частности. Для компьютерных же изданий статья «слишком химическая».
С уважением,
В.Коробов