Расчет противонакипной эффективности ввода затравочных кристаллов в теплоэнергетических установках
Мартынова О.И., доктор техн. наук, Копылов А.С., Кашинский
В.И., кандидат техн. наук, Очков В.Ф., инж.
Для борьбы с накипью на теплопередающих поверхностях при термическом опреснении морской воды и переработки минерализованных сточных вод успешно применяют метод ввода затравочных кристаллов (Л.1-3). Исследования, связанные с применением магнитных аппаратов для таких же целей показали, что при определенных условиях эти устройства генерируют затравочные кристаллы накипеобразователя. Следствием этого процесса является снижение накипеобразования в теплообменнике, использующим воду, прошедшую через магнитный аппарат (Л.4-10).
Несмотря на то, что такой способ борьбы с накипеобразованием (в особенности метод «магнитной обработки» теплоносителя) получил весьма широкое распространение в самых различных областях техники, до сих пор не представлено каких-либо аналитических зависимостей для расчета эффективности ввода затравки. В связи с этим представляет интерес получение количественных соотношений, учитывающих влияние различных факторов на снижение интенсивности отложения накипи на поверхности теплообмена при введении частиц твердой фазы накипеобразователя. Для решения этой задачи рассмотрим материальный баланс вещества в потоке с учетом тепло-массообменных и физико-химических составляющих процесса накипеобразования.
В дифференциальной форме закон сохранения вещества (накипеобразователя) записывается следующим образом:
div j = J - Jт, (1)
где j—плотность потока массы накипеобразователя в растворе, кг/м2с); J—объемная плотность генерации накипеобразователя в растворе, связанная с химическими превращениями, кг/(м3с); Jт— объемная плотность сорбции растворенного накипеобразователя частицами твердой фазы, взвешенными в растворе, кг/м2с).
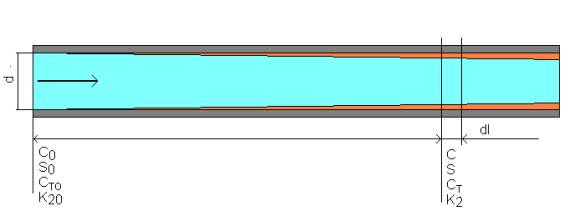
Выражение (1) можно представить в интегральной форме для элементарного объема трубки теплообменника, схематично показанной на рисунке. В этом элементарном объеме раствор пересыщен по накипеобразователю, т. е. его концентрация С выше растворимости S. Это будет вызывать выделение твердой фазы накипеобразователя на внутренней поверхности трубы (накипеобразование) и на поверхности частиц, взвешенных в потоке. Спонтанного образования твердой фазы в толще раствора в данном случае не наблюдается из-за высокого энергетического барьера, связанного с образованием новой фазы.
Закономерности выделения накипи на внутренней поверхности трубы изучены достаточно хорошо [Л. 11—13]. Закон Фика для данного случая преобразуется в выражение:
Jн=rb(С-S), (2)
где jн—плотность потока массы накипеобразователя к внутренней поверхности трубы (интенсивность накипеобразования), кг/м2с); r — плотность раствора, кг/м3; b —коэффициент массоотдачи накипеобразователя к внутренней поверхности трубы, м/с; С—концентрация растворенного накипеобразователя, кг/кг, S—растворимость накипеобразователя, кг/кг.
В критериальной форме формула для определения интенсивности накипеобразования [Л. 13] записывается следующим образом:
NuD=0,023*Re0,8*PrD1/3, (3)
Это выражение достаточно точно описывает закономерности отложения накипи на стенке теплоотдающей трубы в тех случаях, когда интенсивность накипеобразования определяется только стадией
переноса накипеобразователя через диффузионный подслой.
Закономерности выделения накипи на частицах твердой фазы, взвешенных в потоке, изучены намного меньше. Вообще говоря, jт может количественно отличаться от jн, так как при наличии теплового потока от стенки трубы к раствору температура взвешенных частиц ниже температуры слоя накипи. Это сказывается на растворимости накипеобразователя S у слоя накипи на стенке и у поверхности взвешенной в потоке частицы и делает несколько различными концентрационные напоры (С—S) в этих двух случаях.
Кроме того, диффузионный подслой у поверхности взвешенной частицы может быть меньше, чем у поверхности трубы. Интенсивность сорбции накипеобразователя в этом случае будет в большей степени определяться стадией кристаллизации, чем скоростью диффузионных процессов.
Интенсивность сорбции накипеобразователя частицами твердой фазы, находящимися в одинаковых условиях, но имеющих различную кривизну поверхности, может несколько отличаться. Учитывая сказанное, можно записать:
jт=k1*jн, (4)
где jт-плотность потока массы накипеобразователя поверхности частиц твердой фазы накипеобразователя, взвешенных в растворе, кг/(м2с); k1-коэффициент, характеризующий разницу в интенсивностях массоотдачи к поверхности трубы и к поверхности взвешенных частиц твердой фазы накипеобразователя.
В реальных испарительных аппаратах теплообмен осуществляется при относительно малых тепловых нагрузках, при которых температурный напор между теплоотдающей поверхностью и раствором не превышает 2-4 оС. Кроме того, используются режимы, при которых температура раствора и стенки поддерживается в пределах 40-110оС. В этих условиях для расчета интенсивности накипеобразования как на обогреваемых, так и на необогреваемых поверхностях используются одни и те же зависимости (Л.14). Поэтому в рассматриваемом случае можно считать, что k1 не будет существенно отличаться от единицы.
При оценке процессов накипе- и шламообразования важным параметром является отношение суммарной площади частиц твердой фазы накипеобразователя, взвешенных в потоке, к поверхности теплообмена k2. Используя понятие средний эффективный диаметр взвешенных частиц накипеобразователя, можно записать:
k2=1,5Стdr/dтrт , (5)
где k2-отношение суммарной поверхности взвешенных частиц твердой фазы накипеобразователя к поверхности трубы; Ст—концентрация частиц твердой фазы накипеобразователя в растворе, кг/кг; d—диаметр трубы, м; dт средний эффективный диаметр частиц твердой фазы накипеобразователя в растворе, м; rт —плотность твердой фазы накипеобразователя, кг/м3.
Значение k2 не постоянно по длине трубки l. Оценку степени увеличения суммарной поверхности можно сделать следующим образом. Допустим, что в трубку поступает раствор с карбонатной жесткостью, равной Жк, мг-экв/кг. На расстоянии l от входа в трубу некоторая доля карбонатной жесткости a ликвидируется в результате сорбции карбоната кальция на взвешенных частицах. В этом случае изменение параметра k2 можно оценить, используя соотношение
k2/k20=(1+(5*10-5*Жк/Cто)*a)p (6)
где р=1при dт=соnst и р=2/з при постоянном числе частиц.
В табл. 1 представлены расчетные значения k2/k20 при различных a, Ст и р (Жк=4 мг-экв/кг).
Анализ представленных в табл. 1 расчетных данных показывает, что существенное изменение параметра k2, т. е. увеличение суммарной поверхности взвешенных частиц подлине теплообменника, проявляется только при относительно небольших значениях начальной их концентрации. Следовательно, при обеспечении необходимой начальной концентрации .взвешенных частиц в растворе параметр k2 можно с достаточным основанием считать постоянным.
В выражении (1) величина J характеризует степень увеличения концентрации накипеобразователя за единицу времени при протекании химических реакций. Если накипеобразователем является карбонат кальция, это может быть реакция термического разложения бикарбонатов:
2НСО3-®СО32-
+СО2+Н2О, (7)
Записав уравнение (1) в интегральной форме для элементарного участка трубы dl и подставив в него уравнения (2)—(5), получим дифференциальное уравнение, характеризующее процессы накипеобразования на поверхности трубы и шламообразования в объеме:
-dC/dt=0,092/d*Re-0,2*PrD-2/3*(1+k1*k2)*(C-S)-J/r×u, (8)
где v—скорость раствора в трубе, м/с.
С учетом сделанных допущений для теплообменной трубы с незначительным перепадом температур по длине (S=const), при условии, что в поступающем в рассматриваемый объем растворе процесс термического разложения бикарбонатов полностью закончился (J==0), а поверхность взвешенных частиц практически не изменяется (k2=const), решение дифференциального уравнения (8) будет иметь следующий вид:
C-S=(Co-S)exp(-0,092)*Re-0,2*PrD-2/3*(1+k1*k2)*l/d, (9)
В этом случае противонакипный эффект, связанный с наличием взвешенных частиц накипеобразователя в потоке, определяется уравнением
h=1-exp(-0,092*Re-0,2*PrD*k1*k2*l/d), (10)
В табл. 2 представлены расчетные значения параметра h, рассчитанного по уравнению (10), в зависимости от значений параметров k1k2 и РгD:
В работах [Л. 15—17] значения РгD для основных накипеобразователей даются в пределах 200—500. Значения остальных переменных (Rе==50000 и l/d=1000) выбраны в соответствии с условиями эксплуатации в реальных термоопреснительных аппаратах.
Из табл. 2 видно, что существенного противонакипного эффекта в теплообменнике можно достичь в том случае, если поверхность взвешенных частиц в потоке достаточно велика. В то же время необходимо помнить, что чрезмерное увеличение концентрации взвешенных частиц накипеобразователей в потоке приводит к усилению процессов вторичного накипеобразования.
На промышленной опреснительной установке в г. Шевченко для борьбы с накипью успешно применяется метод ввода затравки в виде мелко размолотого мела [Л. 18]. В зависимости от режима работы теплообменника концентрация затравки в питательной воде меняется от 8 до 20 г/кг. Фракционный состав затравки определяется и условий оптимизации ее осаждения в регенерационных отстойниках и, по-видимому, колеблется о 10 до 1000 мкм. Для оценки противонакипного эффекта в опреснителе необходимо определить оптимальное соотношение суммарной поверхности меловой затравки и поверхности теплообменника при заданных значениях концентрации затравки и эффективного диаметра ее частиц. В табл. 3 представлены значения параметра k2, подсчитанные по формуле (5) для этих условий.
Таблица 1. k2/k20, рассчитанное по формуле (6)
|
Начальная концентрация
взвешенных частиц в растворе Ст0.мг/кг |
Значение показателя степени
р |
Значение параметра k2/k20 |
|||
|
Доля карбоната кальция,
сортированного взвешенными частицами a |
|||||
|
0,05 |
О.5 |
1,00 |
|||
|
10000 |
1 2/3 |
1,001 1,001 |
1,010 1,007 |
1,020 1.013 |
|
|
1000 |
1 2/3 |
1,010 1,007 |
1,100 1,066 |
1,200 1,130 |
|
|
100 |
1 2/3 |
1,100 1.066 |
2,000 1,590 |
3,000 2,080 |
|
|
10 |
1 2/3 |
2,000 1.590 |
11,000 4,950 |
21,000 7,600 |
|
Таблица 2. Противонакипный эффект, связанный с
наличие взвешенных частиц накипеобразователя в потоке
|
|
|
РrD |
Противонакипный эффект, h |
||
|
K1/k2= 0,1 |
K1/k2
= 1 |
K1/k2= 10 |
|
|
200 300 500 |
0,03 0,023 0,017 |
0,266 0,210 0,155 |
0,955 0,906 0.814 |
Из сопоставления представленных в табл. 2, 3 значений следует, что практически достигаемый в рассматриваемом опреснителе противонакипный эффект (80%) обеспечивается при значениях среднего эффективного диаметра затравочных частиц около 50 мкм. При этом сорбция накипеобразователя меловой затравкой практически не меняет начального соотношения размеров поверхности затравки и теплообмена (табл. 1).
Определяющее влияние на эффективность ввода затравки дисперсности затравочных кристаллов, а не их химического и кристаллографического состава, подтверждается результатами исследования [Л. 19]. При использовании для ограничения накипеобразования из морской воды затравочных кристаллов в виде ангидрита сульфата кальция с размерами, не превышавшими 125 мкм, и концентрацией 10—20 г/кг авторам [Л. 19] удалось предотвратить выпадение накипи как сульфата, так и карбоната кальция.
Следует отметить, что предложенные выше уравнения получены на основании самых общих представлений о механизме .рассматриваемого процесса. Для получения расчетных зависимостей были приняты некоторые допущения, существенно упрощающие расчеты и придающие их результатам несколько приближенный характер. Учет всех факторов, влияющих на процесс взаимодействия затравки с теплоносителем очевидно возможен только после проведения специальных экспериментальных исследований кинетики кристаллизации накипеобразователя на поверхности затравочных кристаллов различного фракционного состава.
Механизм противонакипной магнитной обработки водных растворов не изучен достаточно полно. Имеются гипотезы, с помощью которых делаются попытки объяснить влияние магнитного поля на накипеобразующую способность технических водных сред. В работе [Л. 20] приведены результаты лабораторных и промышленных экспериментов по изучению механизма противонакипной магнитной обработки, которые доказали обоснованность приведения аналогии между магнитным способом борьбы с накипью и технологией, основанной на вводе затравочных кристаллов. При этом было показано, что при прохождении технических водных растворов, пересыщенных по накипеобразователям, через магнитный аппарат в его зазоре образуется пористый слой продуктов коррозии с хорошо развитой поверхностью, которая генерирует кристаллы накипеобразователя, играющие в теплообменнике роль затравки. Результаты исследования [Л. 20] позволяют рассматривать противонакипную магнитную обработку как комплекс совместно действующих известных технологий водообработки магнитного фильтрования, контактной стабилизации и ввода меловой затравки.
Чтобы принять в качестве рабочей гипотезы утверждение о том, что магнитный аппарат является генератором затравочных кристаллов, необходимо внести следующие положения, которые определяют различия между магнитным способом борьбы с накипью и методом ввода затравки.
При использовании магнитного аппарата затравочные кристаллы вводятся не извне, а образуются самопроизвольно в результате снятия части пересыщения раствора по накипеобразующим компонентам. Таким образом, магнитную обработку можно сравнить с известным способом борьбы с накипью-с контактной стабилизацией, предложенной Ланжелье.
Так как в зазоре магнитного аппарата затравочные кристаллы могут образовываться только вследствие снятия имеющегося пересыщения, то их концентрация в воде, поступающей в теплообменник, не может иметь такие большие значения, как при использовании метода ввода меловой затравки. В случае магнитной обработки концентрация частиц твердой фазы накипеобразователей в воде, поступающей в теплообменник, будет определяться характеристиками воды и магнитного аппарата, временем от начала включения магнитного поля и т. д.
Можно провести оценку работы магнитного аппарата, как генератора затравочных кристаллов накипеобразователя. Допустим в магнитный аппарат поступает вода с карбонатной жесткостью Жк, мг-экв/кг; некоторая доля этой начальной карбонатной жесткости g ликвидируется в результате образования кристаллов карбоната кальция. В табл. 4 представлены расчетные значения отношения поверхности затравки к поверхности теплообмена при различных значениях g и dт при Жк=4 мг-экв/кг и d=37 мм (параметр k2). В работе [Л. 5] указано, что при оптимальном режиме обработки «количество взвешенных частиц размером 1,2—1,5 мкм не превышает 3,0—3,5 мг/кг, а частиц размером меньше 0,5 мкм содержатся не менее 80—85%». Используя эти данные и цифры из табл. 4, можно сделать вывод о том, что в магнитном аппарате в реальных условиях перевод нескольких процентов растворенных накипеобразователей в кристаллическое состояние может создать затравочную поверхность, соизмеримую с поверхностью теплообмена (k2==0,1—8,0).
Таблица 3. Отношение суммарной поверхности меловой затравки
к поверхности теплообмена
|
Суммарный эффективный диаметр частиц, мм |
Отношение поверхности затравки к поверхности теплообмена |
||||||
|
Концентрация затравочных кристаллов, г/кг |
|||||||
|
5 |
10 |
15 |
20 |
||||
|
1,0 0 0,5 0,1 0,05 0,01 |
|
|
0,099 0,198 0,99 1,98 9,90 |
|
0,198 0,396 1,980 3,690 19,800 |
0,297 0,594 2,970 5,940 29,700 |
0,396 0,792 3,960 7,920 39,600 |
Таблица 4. Расчетные
значения параметра k2
при использовании магнитного аппарата в качестве генератора затравочных
кристаллов
|
Средний эффективный диаметр взвешенных частиц dт, мкм |
Отношение поверхности затравочных кристаллов к поверхности теплообмена k2 |
||||
|
Доля карбоната кальции, переводимого в твердое состояние в зазоре магнита g |
|||||
|
0,05 |
0,10 |
0,20 |
0,40 |
||
|
5,00 1,00 0.50 0,10 0,05 |
|
0,040 0,197 0,396 1,982 3,964 |
0,079 0.396 0,793 3,964 7,928 |
0,159 0,793 1,586 7,928 15,857 |
0,317 1,586 3,171 15,857 31,714 |
Концентрация затравочных
кристаллов накипеобразователя при работе магнитного аппарата, как указывалось
ранее, намного ниже, чем при специальном вводе меловой затравки в опреснитель.
Так для условий, указанных в табл. 4, Ст=10 — 80 мг/кг против 8—20 г/кг при
специальном вводе меловой затравки. Используя выражение (6) и табл. 1 можно
утверждать, что при низкой концентрации затравки в питательной воде теплообменника
значение параметра k2,
определяющего эффективность затравки [см. уравнение (10) 11 табл. 2], будет
резко увеличиваться в результате сорбции накипеобразователя. При больших начальных
концентрациях затравки значение параметра k2 по теплообменному тракту практически не меняется
[см. выражение (6) и табл. I]. Отсюда следует, что при одинаковой противонакипной
эффективности магнитной обработки воды и технологии, основанной на вводе
затравки извне, значение параметра k2
питательной воды в первом случае может быть в несколько раз ниже. При расчете
противонакипного эффекта по изложенной методике н выведенному выражению
необходимо оперировать некоторым средним .интегральным значением параметра k2, который
может быть значительно выше начального k20.
Литература:
1.
Исследование предотвращения накипи сульфата кальция с
помощью затравки. - В кн.: Опреснение соленых вод. ЦБНТИ, 1966. Авт.: Е.П. Новиков,
Ф.П. Заостровский, В.Г. Шацило и др.
2.
Стандифорд Ф. Испарение морской воды в длинно-трубных
вертикальных испарителях. - В кн. Определение соленых вод. Изд-во иностр. лит.,
1963.
3.
Апельцин И.Э., Клячко В.А. Опреснение воды. М., «Стройиздат»,
1968.
4.
Миненко В.И. Магнитная обработка воды для охлаждения
конденсаторов паровых турбин. – В кн.: Водоподготовка, водный режим и
химконтроль на паросиловых установках. М., «Энергия», 1978.
5.
Тебенихин Е.Ф. Безреагентные методы обработки воды в
энергоустановках. М., «Энергия», 1977.
6.
Тебенихин Е.Ф., Гусев Б.Т. Обработка воды магнитным полем в
теплоэнергетике. М., «Энергия», 1970.
7.
Мартынова О.И., Гусев Б.Т., Леонтьев Е.А. К вопросу о
механизме влияния магнитного поля на водные растворы солей. – «Успехи
физических наук», 1969, т. 98, вып. 1.
8.
Классен В.И. Омагничивание водных систем. М., «Химия», 1978.
9.
Вопросы теории и практики магнитной обработки воды и водных
систем. Сборник второго всесоюзного совещания. М., «Цветметинформация», 1971.
10.
Вопросы теории и практики магнитной обработки воды и водных
систем. Сборник третьего всесоюзного совещания. Новочеркасск. Изд.
Новочеркасского политехнического института, 1975.
11.
Кашинский В.И., Невструева Е.И., Романовский И.М. Механизмы
отложения на теплоотдающих поверхностях при вынужденном движении монорастворов.
– «ИФЖ», 1975, т. 28, № 3.
12. Hasson D., Sherman H., Biton M. Prediction of calcium
carbonate scaling rates. – «Proc. 5 th Intern. Symposium Fresh Water from Sea»,
1978, vol. 2, p. 193-199.
13.
Карнаухов Л.П., Чернозубов В.Б., Васина Л.Г. Закономерности
отложения карбонатной накипи на теплообменных поверхностях в условиях нагрева
природных вод. – «Вопросы атомной науки и техники. Опреснение соленых вод».
Свердловск, 1977, № 2/10.
14.
Гонионский В.Ц. Исследование кинетики отложения накипи
сульфата кальция на поверхности теплообмена.
– Автореф. дис. на соиск. учен. степени канд. техн. наук, М., 1968 (МЭИ).
15. Zanker A. Nomografs for the diffusivities of saits, acids
and bases in very dilute water solution. – «J. of Electrochemical Soc.», 1971, №1.
16.
Хоблер Т. Массопередача и абсорбция. Л., «Химия», 1964.
17.
Бубен Н.Я., Франк-Каменецкий Д.А. Об абсолютных скоростях
растворения. – «ЖФХ», 1946, т. 20, № 3.
18.
Слесаренко В.Н. Современные методы опреснения морских и
соленых вод. М., «Энергия», 1973.
19. Etude de la prevention simultanee des depots de
carbonate de calcium et de sulfate de calcium par germination de l’eau de mer. –
«Proc. 4 th Intern. Symposium Fresh Water from Sea», 1973, vol. 2, p. 47-56.
Auth.: P. Charuit, R. Marchand, M. Viard a. o.
20.
К механизму влияния магнитной обработки на процессы
накипеобразования и коррозии. – «Теплоэнергетика», 1979, № 6. Авт.: О.И.
Мартынова, А.С. Копылов, Е.Ф. Теребенихин, В.Ф. Очков.