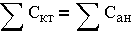
|
или
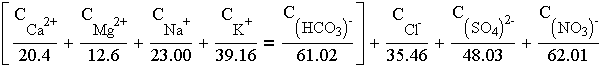
| (2.1.) |
где в числителе приведены массовые концентрации ионов, а в знаменателе, соответствующие эквивалентные массы. Если правая и левая части приведенного равенства различаются менее чем на 1 %, анализ можно считать выполненным правильно. В уравнение (2.1) не следует включать анион -------Н5Юз-------, так как в левой части отсутствует соответствующая концентрация иона водорода, а также оксиды Аl2О3 и Fе2O3, не присутствующие, как правило, в ионной форме.
Показатель концентрации водородных ионов (рН) воды характеризует реакцию воды (кислая, щелочная, нейтральная) и учитывается при всех видах обработки воды.
В соответствии с законом действующих масс для воды, частично диссоциирующей на ионы Н+ и ОН-, согласно уравнению:
| H2O=H++OH- | (2.2.) |
можно записать
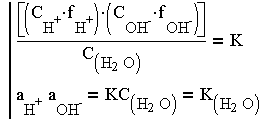
| (2.3.) |
Константа KH2O, или, как ее часто обозначают, KW, называется ионным произведением воды. При диссоциации воды, не содержащей посторонних примесей, ионы Н+ и ОН- образуются в равных молярных (грамм - ионных) концентрациях, в связи с этим активность каждого из них согласно уравнению (2.3.):
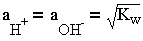
| (2.4.) |
и составит при 22°С 10-7 моль/кг, рН такой нейтральной воды равно 7, в то время как при более высокой температуре рНt той же нейтральной воды будет иным. В природных водах, содержащих бикарбонат - ионы, рН воды можно вычислить, преобразовав уравнение (1.5) к виду:
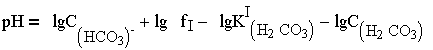
| (2.5.) |
Значение рН водных растворов определяет интенсивность диссоциации содержащихся в них слабых кислот или оснований. С понижением рН, т.е. с повышением активности (или концентрации) ионов Н+, процентное содержание недиссоциированных молекул слабых кислот повышается, а содержание их анионов понижается (табл. 2.3), для катионов слабых оснований наблюдается обратное соотношение. рН природной воды обычно колеблется в пределах 6-8 и зависит в основном от соотношения в воде концентраций НСО3 и Н2СО3. Измерение рН основано на определении разности электрических потенциалов (потенциометрический метод) двух помещенных в анализируемый раствор электродов - индикаторного и электрода сравнения.
Удельная электрическая проводимость растворов X, характеризуемая электрической проводимостью 1см3 (1м3) жидкости с размером граней 1см (1м) и выражаемая в См/см (См/м), является важным показателем качества природной и обработанной воды, указывающим на суммарную концентрацию ионогенных примесей. Удельная проводимость воды, не содержащей примесей, при 25°С составляет 0,063 мкСм/см и определяется переносом в электрическом поле только ионов Н+ и ОН-. Удельная проводимость водных растворов, т. е. проводников второго рода, зависит от температуры, концентрации и типа электролита, степени его диссоциации и скорости движения ионов и измеряется методами кондуктометрии.
При постоянной температуре и данной степени диссоциации существует прямая зависимость между концентрацией электролита и его удельной электрической проводимостью. Так, удельную электрическую проводимость водных растворов различных солей концентрацией до 500 мг/кг в условном пересчете на NaCI можно примерно оценить из соотношения:
| 1 мкСм/см = 0.5 мг NaCl/кг H2O. | (2.5.) |
2.4. Технологические показатели качества воды
Сухой остаток определяют, упаривая 1л профильтрованной воды, подсушивая остаток при 105 °С и взвешивая его. При этом необходимо учитывать, что в указанных условиях термический распад бикарбонатов протекает в соответствии с уравнением (1.9) с выделением С02, т.е. вместо каждых 122 мг бикарбонатионов в составе сухого остатка остается 60 мг карбонатионов. В реальных условиях сухой остаток может оказаться несколько больше расчетного значения солесодержания (т.е. суммы концентраций отдельных ионов) из - за того, что некоторые соли при температуре 105°С удерживают часть кристаллизационной воды и в сухом остатке присутствуют коллоидные, в том числе и органические, примеси. Поэтому сухой остаток нужно рассматривать как показатель, лишь приближенно характеризующий загрязненность воды и дающий порядок его величины.
Плотный осадок, определяют, подсушивая при 105°С упаренный остаток нефильтрованной воды, содержащей также и грубодисперсные примеси, концентрацию которых можно найти по разности плотного и сухого остатков воды.
Общей щелочностью воды, (Що), мг - экв/кг, называют сумму миллинормальных концентраций всех анионов слабых кислот и гидроксильных ионов за вычетом концентрации ионов водорода:
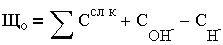
| (2.7.) |
В зависимости от типа анионов, обусловливающих щелочность, различают щелочность бикарбонатную - ЩБ (НСО3-), карбонатную - ЩК(CO3-), силикатную - ЩС(НSi3-,SiO32-), гидратную - ЩГ (ОН-), фосфатную - ЩФ(Н2Р04, НР042-, Р04-):
| ЩO=ЩБ+ЩК+ЩС+ЩФ+ЩГ | (2.8.) |
В большинстве природных вод концентрация бикарбонат - иона преобладает над концентрациями других анионов слабых кислот, поэтому общая щелочность обычно численно совпадает с концентрацией бикарбонатов, выраженной в единицах мг - экв/кг.
Так как аналитически достаточно надежно определенным значением щелочности можно считать. 10-5н. (0,01 мг - экв/кг), учет гидратной щелочности следует проводить лишь при концентрации ионов ОН->10-5 н., т.е. при рН>9.
Экспериментально щелочность определяют титрованием пробы воды кислотой в присутствии кислотно - щелочных индикаторов, меняющих свою окраску при различных значениях рН. Как видно из табл.2.3, в случае использования индикаторов, меняющих свою окраску при рН=8,2 (фенолфталеин) и рН=4,4 (метиловый оранжевый), при титровании легко идентифицировать бикарбонатную гидратную и карбонатную щелочность. Обозначая через Ф количество израсходованной кислоты при титровании по фенолфталеину и через М суммарный расход кислоты по фенолфталеину и метиловому оранжевому с учетом мольных переходов CO32- НСО3- Н2СО3, получаем данные для определения вида щелочности ЩО ЩК, ЩГ (табл. 2.4).
| Ингридиент | Допустимая концентрация, мг/кг | Лимитирующий показатель | Норма для рыбохозяйственных водоемов, мг/кг |
|---|---|---|---|
| Ванадий | 0.1 | СТ | --- |
| Гидрозин | 0.01 | СТ | --- |
| Медь | 1.0 | ОС | 0.001 |
| Магний | --- | ОЛ | 40.00 |
| Медь многосернистая | 0.1 | ОЛ | 0.05 |
| Нефть прчная | 0.3 | ОЛ | 0.05 |
| Полиакриламид | 2.0 | СТ | --- |
| Хлор активный | Отсутствует | ОС | Отсутствует |
| Сульфиды | --- | ОС | --- |
| Трилон Б | --- | СТ | 0.5 |
Жесткость воды - один из важнейших показателей ее качества, Общей жесткостью (ЖO) называют суммарную концентрацию ионов кальция и магния, выраженную в эквивалентных единицах (мг - экв/кг, а при очень малых значениях - в мкг - экв/кг). Общую жесткость воды подразделяют на кальциевую и магниевую. Часть ЖO (в предельном случае при ЩO > ЖO вся жесткость), эквивалентная содержанию бикарбонатов, называется карбонатной жесткостью; разность между общей и карбонатной жесткостями называется некарбонатной жесткостью.
Процесс выделения из воды ионов Са2 и Mg2 получил название умягчения воды. Воды с высокой жесткостью, дают плотные отложения на теплопередающих поверхностях.
По значению общей жесткости природных вод установлена следующая классификация: ЖO<1,5 мг - экв/кг - малая жесткость, ЖO=1.5 - 3.0 мг-экв/кг - средняя, ЖO=3,0 - 6,0 мг-экв/кг - повышенная, Жо=6,0 - 12,0 мг-экв/кг - высокая, ЖO>12 мг-экв/кг - очень высокая жесткость.
Окисляемость воды - это показатель, имеющий условное значение и представляющий собой расход какого-либо сильного окислителя, необходимого для окисления в определенных условиях органических примесей, которые содержатся в 1 л воды. Обычно для этих целей применяют перманганат калия (КМnO4) или бихромат калия (К2Сг2О7), различая соответственно перманганатную и бихроматную окисляемость. Результаты определения перманганатной окисляемости воды выражают в кислородных или перманганатных единицах (O2, КМn04, мг/кг), различающихся в 3,95 раза. Бихроматная окисляемость обычно превышает в 2 - 2,5 раза перманганатную, а разность между ними позволяет судить об устойчивости органических примесей к действию окислителей. При определении окисляемости обоих видов происходит окисление не только содержащихся в воде органических веществ, но и некоторых неорганических, например закисного железа, сероводорода, нитритов. Поэтому следует еще раз подчеркнуть, что окисляемость характеризует содержание в воде органических веществ лишь приближенно и условно.
Окисляемость чистых грунтовых вод составляет обычно 1-3 мг 02/кг, в то время как в водах поверхностных источников окисляемость повышается до 10 - 12 мг 02/кг. Реки болотного происхождения и поверхностные источники, в период паводка отличаются очень высокой окисляемостью, превышающей, например, 30мг 02/кг. Сточные воды, содержащие органические вещества и сбрасываемые в водоемы, могут повышать окисляемость воды различных источников.
Для суммарной оценки органических загрязнений воды в последнее время начинают применять метод сорбции из воды органических веществ активированным углем с последующим его высушиванием и экстракцией из него этих веществ хлороформом (метод угольно - хлороформного экстракта). В массовых единицах (мг/кг) оценивают в ряде случаев содержание общего органического углерода в воде.
Концентрация растворенных газов в воде зависит от их природы, температуры воды и парциального давления, типа и концентрации минеральных и органических примесей воды, рН воды и т.п. Характеристика процессов выделения и поглощения газов изложена в гл. 17.
2.5. Биологические показатели качества воды
В некоторых случаях химикам - теплоэнергетикам приходится готовить воду так называемого питьевого качества для систем открытого горячего водоснабжения либо использовать для водоснабжения и сброса стоков ТЭС открытые водоемы, служащие также и для питьевого водоснабжения, в связи с чем необходимо иметь представление и о некоторых биологических качествах воды. Вода - среда для развития многочисленных форм вирусов, бактерий, простейших и сложных организмов. К числу бактериальных и вирусных водных инфекций относятся дизентерия, брюшной тиф, холера, полиомиелит, бруцеллез и др.
Для определения чистоты воды в качестве критерия выбрана кишечная палочка. Кишечные палочки отмирают в воде медленнее многих болезнетворных бактерий, поэтому уничтожение кишечных палочек в процессе обеззараживания воды гарантирует в значительной мере отсутствие болезнетворных бактерий. Количество кишечных палочек в воде выражается коли-титром (к - т), т.е. тем объемом воды в 1 см3, в котором содержится одна кишечная палочка, или коли-индексом (к-и) - количеством кишечных палочек в 1 кг воды. Согласно ГОСТ для питьевой воды коли-титр должен быть не менее 300 (или коли - индекс не более 3).
В поверхностных водоемах находится также большое количество водорослей и микроорганизмов. Совокупность водорослей и микроорганизмов, обитающих в объеме воды, называется соответственно фито- и зоопланктоном, организмы, населяющие дно водоемов, называются бентосом. Питьевая вода не должна содержать живых и мертвых планктонных организмов, продуктов обмена веществ и распада клеток этих организмов. Обеспечение этого условия осложняется при так называемом цветении воды, т. е. массовом развитии планктона. Применение воды, содержащей планктон, затрудняет нормальное протекание процесса ее обработки для целей промышленного использования. В отечественной практике водоподготовки цветность воды принято определять сравнением со стандартной платиново - кобальтовой шкалой и выражать результат измерения в градусах этой шкалы. Запах и вкус оцениваются количественно по пятибалльной системе.
В заключение отметим, что содержание в природных водах примесей различной степени дисперсности вызывает необходимость очистки ее в несколько стадий. На первом этапе из воды удаляются коллоидные и грубодисперсные вещества, на последующих - ионодисперсные вещества и растворенные газы. Такой системный подход к выбранной последовательности технологических приемов обработки воды связан с оптимизацией технико - экономических показателей различных стадий очистки, с возможностью автоматизации работы отдельных аппаратов и повышения надежности работы водоподготовительной установки (ВПУ) в целом. Например, коллоидные примеси органических веществ в природных водах могут вызвать ухудшение показателей анионообменной части ВПУ ("старение" анионитов, увеличение удельных расходов щелочи при регенерации), а коллоидные соединения железа могут быть причиной отравления ионитных мембран в электродиализных аппаратах. Неэффективная очистка добавочной воды от коллоидных и грубодисперсных веществ является одной из причин образования отложений на поверхностях нагрева и коррозии поверхности элементов проточной части турбин, что характеризует важность первого этапа очистки воды от коллоидных и грубодисперсных примесей, называемого предочисткой.
Предочистка осуществляется на основе методов, в результате реализации которых при дозировке специальных реагентов некоторые примеси выделяются из воды в виде хлопьев, имеющих размеры 0.1 - 1 мм. Основными технологическими процессами предварительной очистки воды являются коагуляция (укрупнение) коллоидных примесей и известкование, которые обычно совмещаются одновременно в одном аппарате - осветлителе в целях улучшения суммарного технологического эффекта и снижения денежных затрат. Дополнительная очистка воды после осветлителей от грубодисперсных примесей производится фильтрационными методами, которые также относятся к предочистке воды.
Вопросы и предложения направляйте в службу поддержки